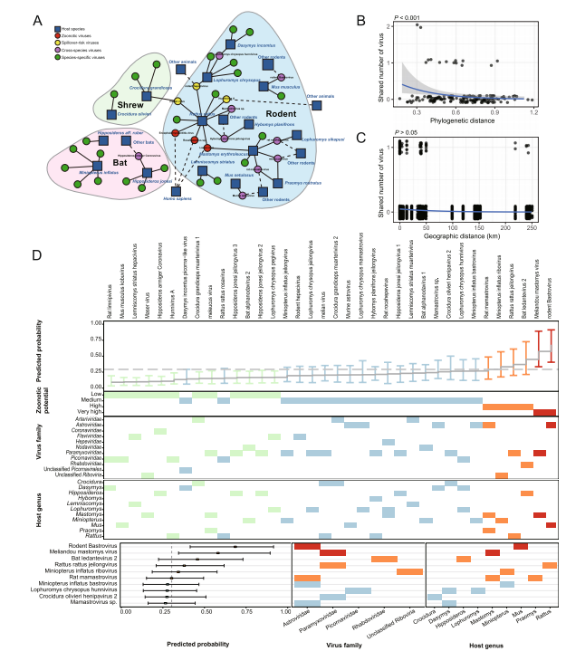
En nyligen publicerad studie iMikrobiomutförde viral metagenomisk analys på 846 vilda små däggdjur – inklusive fladdermöss, gnagare och näbbmöss – insamlade i Sierra Leone, Västafrika. Studien identifierade totalt 39 däggdjursassocierade RNA-virus, bestående av 26 nya och 13 tidigare kända virus. Bland dessa uppvisade familjen Paramyxoviridae den högsta mångfalden, medan gnagare hyste det största antalet virusarter (n = 26).
Zoonotisk riskbedömning avslöjade tre kända zoonotiska virus – encefalomyokarditvirus, Lassavirus och Rocahepevirus sp. – samt tre virus med potentiell spridningsrisk: Melianvirus, gnagarhepatitvirus och Hunnivirus A. Bland de nyligen identifierade virusen uppvisade Bat ledantevirus 2 det närmaste fylogenetiska släktskapet med det mänskligt infekterande Le Dantec-viruset. Serologisk analys upptäckte vidare neutraliserande antikroppar mot detta virus hos 2,8 % av de lokala invånarna, vilket tyder på tidigare, sannolikt oupptäckt, mänsklig exponering.
Dessa fynd belyser förekomsten av en betydande gnagardominerad virusreservoar i Västafrika och understryker den kritiska vikten av integrerade övervakningsstrategier i gränssnittet mellan människa och djur. Att kombinera metagenomisk screening med serologisk validering ger ett robust ramverk för att identifiera virus med zoonotisk och spillover-potential.

Under det senaste decenniet har mer än 60 % av de nya infektionssjukdomarna hos människor sitt ursprung i djurreservoarer, där fladdermöss, gnagare och näbbmöss är viktiga värdar för zoonotiska virus. Afrika anses allmänt vara ett hotspot för zoonotiska sjukdomar. Till exempel rapporterade Sierra Leone över 28 000 fall under ebolautbrottet 2014–2016.
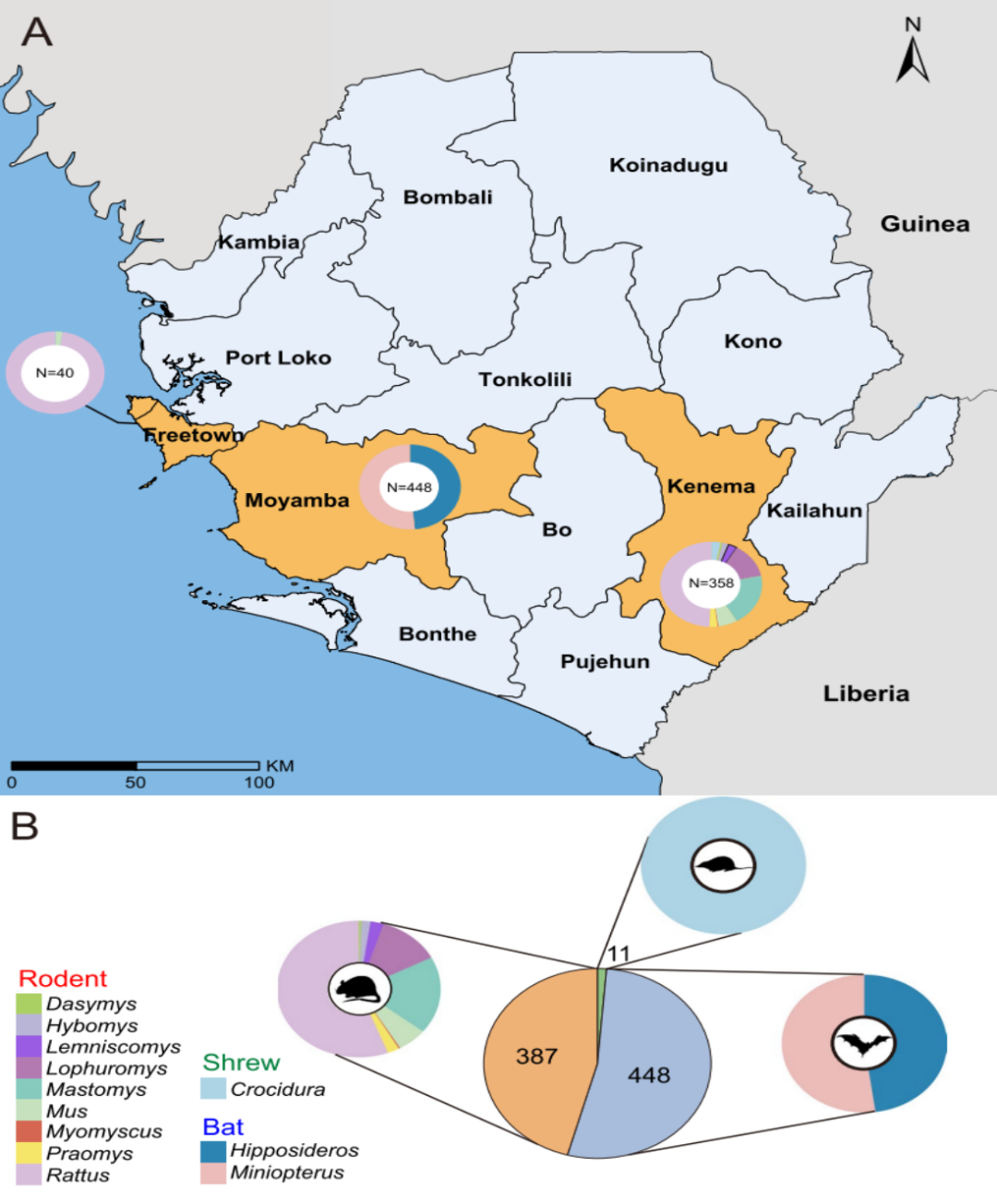
Trots den betydande belastningen av zoonotiska sjukdomar i denna region är mångfalden och spridningen av virus hos vilda små däggdjur fortfarande otillräckligt karaktäriserad. För att åtgärda denna brist genomförde forskare en systematisk viromanalys av 846 vilda små däggdjur som fångats på tre platser i Sierra Leone mellan 2018 och 2023. Studien syftade till att karakterisera virusmångfalden, identifiera kandidater med potential för överföring mellan arter, bedöma zoonotisk risk och generera bevis för att stödja tidiga varningssystem för nya infektionssjukdomar.
Kärnmetoder
Studien tillämpade ett omfattande arbetsflöde för viral metagenomik:
- Provbearbetning:Hjärt-, lever-, mjälte-, lung- och njurvävnader samlades in, poolades, homogeniserades och utsattes för total RNA-extraktion.
- Sekvensering och montering:Ribosomalt RNA-utarmning utfördes före bibliotekskonstruktion, följt av högkapacitetssekvensering med hjälp av Illumina NovaSeq 6000-plattformen. Virala contigs sattes samman de novo.
- Virusidentifiering:Virus identifierades baserat på RNA-beroende RNA-polymeras (RdRp) geninriktning. Endast ryggradsdjursassocierade virus behölls, exklusive bakterie-, svamp- och växtvirus.
- Bioinformatisk analys:Fylogenetisk rekonstruktion, rekombinationsanalys, modellering av överföringsnätverk mellan arter och zoonotisk riskbedömning genomfördes.
- Serologisk validering:En VSV-baserad pseudovirusneutraliseringsanalys utvecklades för Bat ledantevirus 2. Neutraliserande antikroppar detekterades i 2,8 % av humant serum, vilket ger bevis på potentiell zoonotisk överföring.
StuderaResultat
1. Viral upptäckt och mångfald
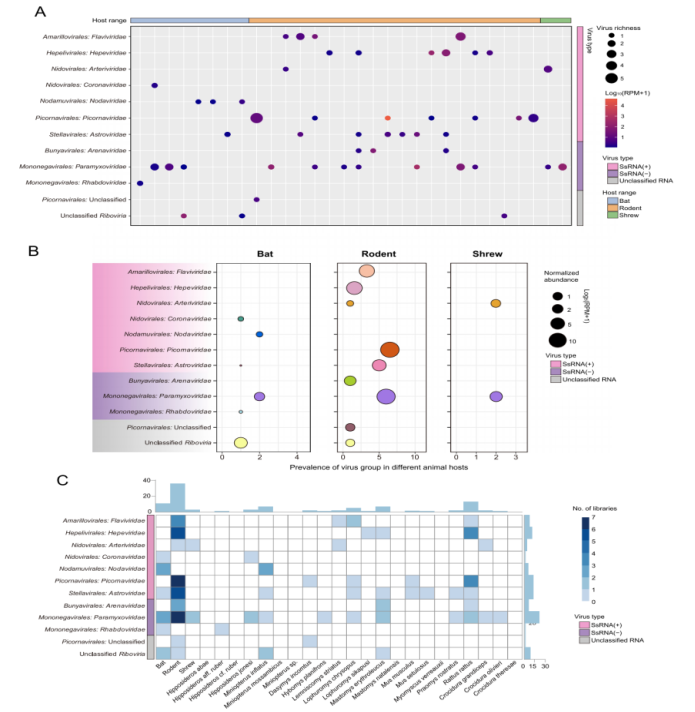
Denna studie utförde transkriptomisk sekvenseringsanalys på 846 vilda djur insamlade i Sierra Leone, inklusive gnagare, fladdermöss och näbbmöss. Baserat på kompletta RNA-beroende RNA-polymeras (RdRp) gensekvenser identifierades totalt 39 däggdjursassocierade RNA-virus, bestående av 13 tidigare kända virus och 26 nya virus.
När det gäller virussammansättning uppvisade familjen Paramyxoviridae den högsta nivån av mångfald inom alla tre värdordnare, följt av Astroviridae och Picornaviridae. När det gäller värddistribution bidrog gnagare med den största virusmångfalden och härbärgade totalt 26 virusarter, vilket indikerar deras framträdande roll som reservoarer för virusmångfald i regionen.
2. Zoonotisk risk
Zoonotisk riskbedömning identifierade tre kända zoonotiska virus: encefalomyokarditvirus, Lassavirus och Rocahepevirusarter. Dessutom identifierades tre virus – Melianvirus, gnagarhepatitvirus och Hunnivirus A – som potentiellt smittade.
Bland de 26 nyupptäckta virusen förutspåddes fyra ha hög zoonotisk potential baserat på fylogenetiska och genomiska egenskaper. Det är värt att notera att Bat ledantevirus 2 uppvisade det närmaste fylogenetiska släktskapet med det kända mänskligt infekterande Le Dantec-viruset.
Efterföljande serologisk undersökning stödde ytterligare detta fynd, då neutraliserande antikroppar mot Bat ledantevirus 2 detekterades i 2,8 % av serum från lokala invånare. Detta resultat tyder på att oupptäckta eller asymptomatiska infektioner redan kan ha inträffat inom den mänskliga populationen, vilket belyser en potentiell men tidigare oupptäckt zoonotisk överföringsväg.
3. Dynamik i överföring mellan arter
Analys av spridning mellan arter visade att gnagare intar en central position inom det virala nätverket, och fungerar som viktiga noder som underlättar virusutbyte mellan värdarter. Totalt 15 virus identifierades som ha potential för spridning mellan arter.
Ytterligare analys av överföringsmönster mellan olika ordningar indikerade att virusdelning förekom oftare mellan värddjur inom samma taxonomiska ordning, vilket tyder på att värddjurssläktskap spelar en viktig roll i överföringsdynamiken. Däremot uppvisade fladdermöss en relativt lägre kapacitet för överföring mellan olika ordningar.
Viktigt är att bevis på värdutbredning observerades hos vissa virus. Till exempel upptäcktes även Melianvirus, som tidigare ansetts specifikt för näbbmöss, hos gnagare i denna studie, vilket indikerar en potentiell förändring i värdens anpassningsförmåga och en ökad risk för bredare överföring.
Slutsatser och folkhälsokonsekvenser
- Hög viromdiversitet hos vilda små däggdjur:Upptäckten av 39 RNA-virus, inklusive 26 nya arter, avslöjar en stor virusreservoar i regionen och rapporterar för första gången nya virus med hög zoonotisk potential (t.ex. Bat ledantevirus 2).
- Gnagare som prioriterade övervakningsmål:Gnagare fungerar som viktiga nav för virusöverföring och bär på den högsta virala mångfalden, vilket representerar den största spridningsrisken.
- Behov av integrerade övervakningsstrategier:Resultaten stöder prioritering av gnagare i aktiva övervakningsprogram och implementering av integrerade metoder som kombinerar metagenomik, serologi och ekologisk övervakning i gränssnittet mellan människor och vilda djur.
Sammantaget ger denna studie viktiga bevis som stöd för tidiga varningssystem och riskbedömningsramverk för nya zoonotiska sjukdomar, vilket förstärker vikten av proaktiv övervakning i högriskregioner.
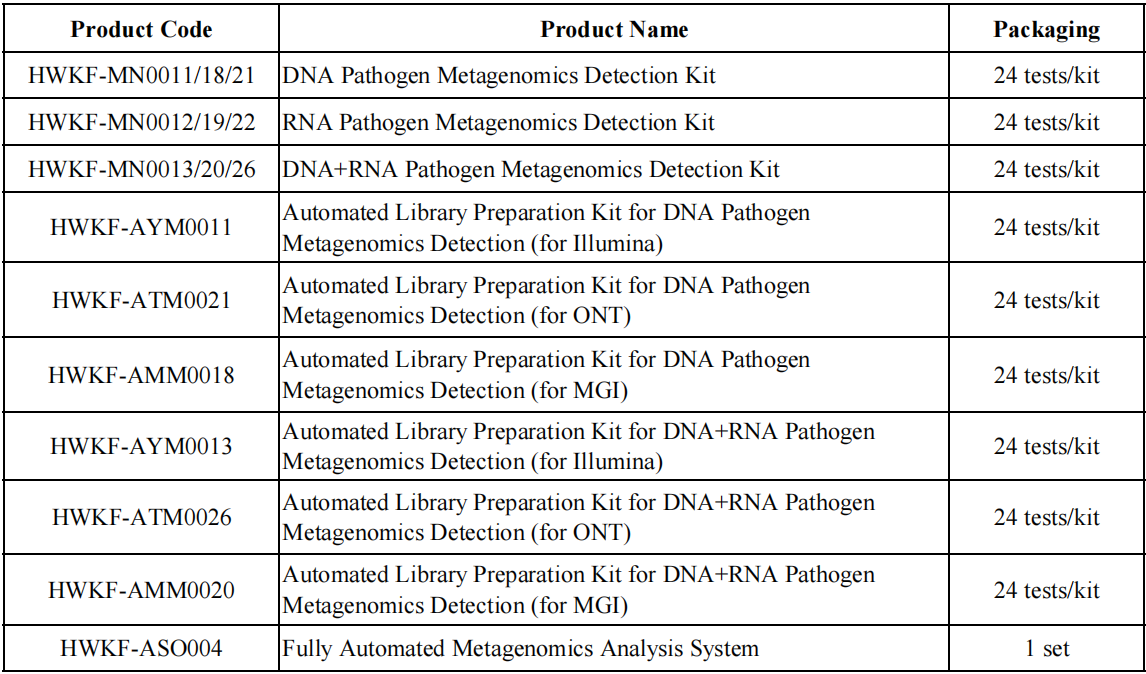
Produktinformation
Publiceringstid: 23 mars 2026