- 1. Global börda av livmoderhalscancer och screeningutmaningar
Livmoderhalscancer är fortfarande en stor global folkhälsoutmaning, trots att den till stor del kan förebyggas genom effektiv screening och tidiga insatser. Enligt Världshälsoorganisationen (WHO) inträffade uppskattningsvis 662 000 nya fall och 349 000 dödsfall världen över under 2022, vilket rankar den som den fjärde vanligaste cancerformen och den fjärde ledande orsaken till cancerrelaterad dödlighet bland kvinnor. Sjukdomsbördan är oproportionerligt koncentrerad till låg- och medelinkomstländer (LMIC), där incidensen och dödligheten är betydligt högre än i höginkomstländer. De beror främst på bristen på högkvalitativa screeningprogram och effektiv upptäckt och behandling av precancerösa lesioner, vilket förvärras av:
-Bristfällig eller svag screeninginfrastrukturBrist på tillgängliga, kvalitetssäkrade screeningtjänster.
-ResursbegränsningarBegränsad laboratorieinfrastruktur, kylkedjelogistik och pålitlig elektricitet.
-Brist på arbetskraftBrist på utbildad laboratorie- och klinisk personal.
-Förseningar och förlust av uppföljningFördröjning mellan provtagning och tillgängligheten av resultat, vilket leder till förseningar i klinisk behandling eller att patienter går förlorade för uppföljning[1].
2. Etiologi och molekylär grund för cervikal karcinogenes
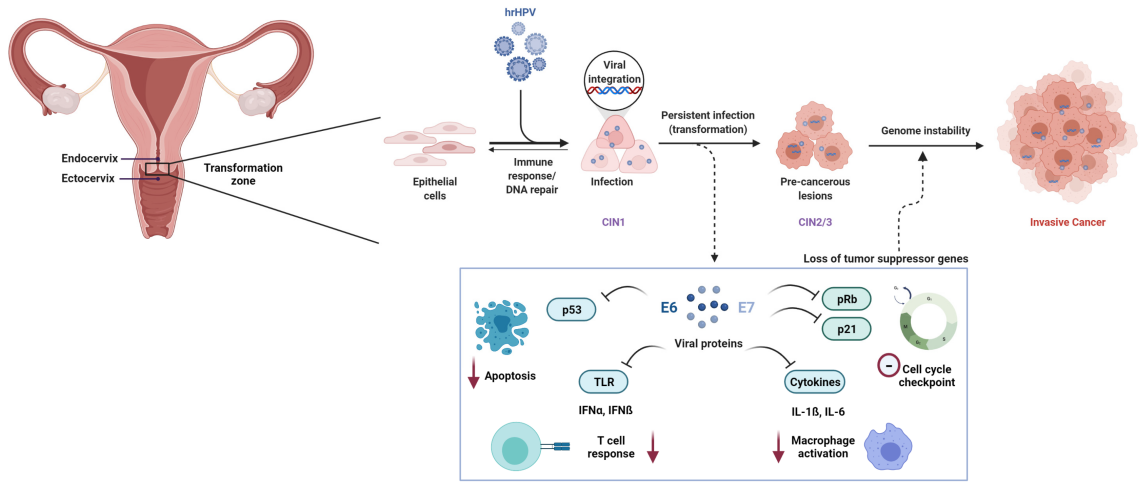
Ihållande infektion med högrisk-humant papillomvirus (HR-HPV) är en nödvändig orsak till livmoderhalscancer. Bland mer än 200 identifierade HPV-genotyper finns minst12 typerhar klassificerats som cancerframkallande (grupp 1) av Internationella byrån för cancerforskning (IARC).

På molekylär nivå drivs HPV-medierad karcinogenes primärt av de virala onkoproteinerna E6 och E7. E6 främjar nedbrytningen av tumörsuppressorproteinet p53, medan E7 funktionellt inaktiverar retinoblastomproteinet (Rb), vilket resulterar i dysreglering av cellcykeln och malign transformation.
3.WHO-rekommenderade screeningstrategier
Världshälsoorganisationen rekommenderar HPV-nukleinsyratestning (NAT) som den föredragna primära screeningmetoden för att förebygga livmoderhalscancer.
Allmän befolkning:HPV-DNA- eller mRNA-baserade NAT:er
Kvinnor som lever med hiv:HPV-DNA-baserade NAT:er
Screeningsintervall:
Kvinnor i åldern 30–65 år: Vart 5–10 år
Kvinnor som lever med hiv: Vart 3–5 år
Jämfört med cytologibaserade metoder visar HPV-testninghögre känslighetoch tillhandahållerett överlägset negativt prediktivt värde, vilket möjliggör längre och mer kostnadseffektiva screeningsintervall.
4.WHO:s målproduktprofil för HPV-screeningtester
WHO har utvecklat enMålproduktprofil (TPP)för HPV-screeninganalyser avsedda för användning i decentraliserade och resursbegränsade miljöer.[1]
Viktiga egenskaper inkluderar:
- Kompatibilitet med självinsamlade prover
- Detektion av flera högrisk-HPV-genotyper (≥12 typer)
- Användning av icke-laboratorieutbildad personal
- Resultat tillgängliga inom ett enda kliniskt möte
Dessa kriterier stöder vårdnära testning och ”screen-and-treat”-strategier.
5.En helautomatiserad plattform för detektion av högrisk-HPV
Macro & Micro-Tests AIO800-system gerett helt automatiserat arbetsflöde från exempel till svarintegrering av nukleinsyraextraktion, amplifiering och detektion i linje med WHO:s rekommenderade screeningstrategier.

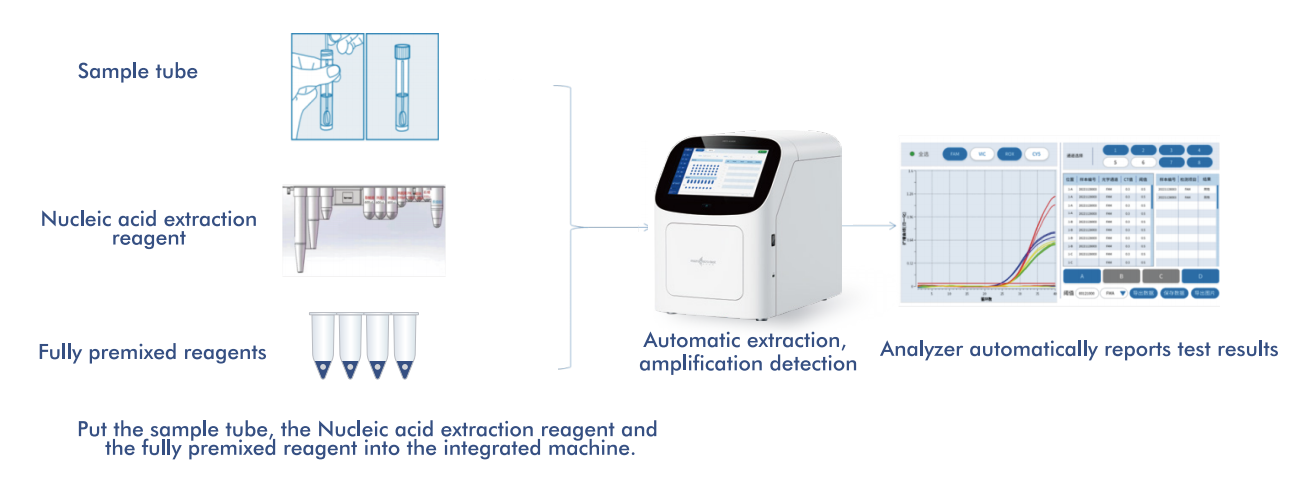
5.1 Automatiserat arbetsflöde från prov till svar
Plattformen integrerar extraktion, amplifiering och detektion av nukleinsyra i ett enda, slutet system, vilket kräver minimal operatörsingripande. Denna design:
- -Minskar beroendet av specialiserad laboratoriepersonal
- -Minimerar processvariationer och kontamineringsrisk
- -Möjliggör implementering i decentraliserade vårdmiljöer
Samtidigt stöder dess genomströmningskapacitet tillämpning i centraliserade laboratorier, vilket underlättar storskaliga screeningprogram.
5.2 Bred genotypningstäckning
Systemet detekterar 14 högrisk-HPV-typer, inklusive alla 12 cancerframkallande typer som klassificerats av IARC (HPV16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58 och 59), samt HPV66 och HPV68.
Viktigt är att det gertypspecifik genotypningresultat, vilket möjliggör riskstratifiering och mer exakt klinisk hantering.
5.3 Analytisk känslighet och kliniska implikationer
Med en detektionsgräns på 300 kopior/ml kan systemet identifiera låggradig HPV-infektion som bidrar till:
- -Tidigare upptäckt av kliniskt relevanta infektioner
- -Förbättrat negativt prediktivt värde
- -Stöd för förlängda screeningsintervall
5.4 Stöd för självprovtagning
Plattformen är kompatibel med bådacervixprover och självtagna urinproveri linje med WHO:s rekommendationer för att ta itu med viktiga hinder för screening, inklusive:
- -Begränsad tillgång till vårdinrättningar
- -Sociokulturella begränsningar
Publiceringstid: 27 mars 2026
