1 Bakgrund till dengueepidemin: En eskalerande global folkhälsoutmaning
Dengue är en akut myggburen virussjukdom orsakad av dengueviruset (DENV), som har framstått som den snabbast spridande arbovirussjukdomen globalt och utgör ett betydande hot mot folkhälsosäkerheten. Under de senaste två decennierna har den globala incidensen av dengue ökat dramatiskt, med antalet rapporterade fall som fördubblats årligen sedan 2021 [1]. I december 2023 utlyste Världshälsoorganisationen (WHO) ett globalt nödläge för dengue för att stärka samordnade internationella insatser. Epidemiologiska uppskattningar från WHO visar att cirka 3,9 miljarder individer världen över riskerar att drabbas av dengueinfektion, med uppskattningsvis 390 miljoner infektioner som inträffar årligen – varav 96 miljoner uppvisar kliniskt synliga fall [1,2].
2 Epidemiologiska höjdpunkter
De epidemiologiska egenskaperna hos denguefeber formas av samspelet mellan virologiska faktorer, vektorekologi, värdens immunsvar och socio-miljömässiga förhållanden. En omfattande förståelse av dessa egenskaper är avgörande för utvecklingen av effektiva förebyggande och kontrollstrategier samt korrekta diagnostiska metoder.
2.1 Transmissionsvektorer och urbana transmissionsmönster
Dengueviruset överförs främst viaAedes aegypti och Aedes albopictusmyggor. Bland dessa vektorarter är Aedes aegypti erkänd som den mest kritiska överföringsvektorn, kännetecknad av hög "mänsklig anpassningsförmåga" och utbredd spridning i tropiska och subtropiska stadsmiljöer. Till skillnad från andra myggvektorer av arbovirala patogener uppvisar Aedes aegypti följande viktiga epidemiologiska egenskaper:
-En preferens för avel i antropogena miljöer (t.ex. vattenbehållare, kasserade däck)
-En stark tropism för mänskligt blod som näringskälla
-Ätningsbeteende under dagtid
Dessa egenskaper definierar denguefeber som en typisk"smittsam sjukdom i städerna"med en signifikant ökad överföringseffektivitet i tätbefolkade områden. WHO-relaterade studier har visat att i tätbefolkade stadsmiljöer kan ökad frekvens av kontakt mellan myggor och människor avsevärt höja det grundläggande reproduktionstalet (R₀) för DENV, vilket påskyndar spridningen av epidemier [2].
2.2 Globala spridningstrender och drivande faktorer
Enligt WHO-rapporter har det globala antalet rapporterade denguefall ökat exponentiellt under de senaste två decennierna [1,3]. Denna uppåtgående trend drivs främst av följande sammankopplade faktorer:
(1) Klimatförändringar: Stigande globala temperaturer utökar inte bara det geografiska utbudet av lämpliga livsmiljöer för myggvektorer utan förkortar också den yttre inkubationsperioden för DENV inom myggvärden, vilket förbättrar överföringseffektiviteten. Klimatinducerade variationer i myggtäthet har validerats av WHO som en tillförlitlig prediktor för den spatiotemporala dynamiken i dengueutbrott.
(2) Urbanisering: Snabb och oplanerad stadsexpansion har skapat rikliga häckningsmiljöer för myggvektorer, medan ökad befolkningstäthet har stärkt kontinuiteten i DENV-smittkedjorna.
(3) Globala befolkningsrörelser: Internationella resor och handel har underlättat den snabba gränsöverskridande överföringen av DENV, vilket främjar övergången från importerade fall till ihållande lokal överföring. WHO:s övervakningsdata visar att mellan 2010 och 2021 rapporterade USA 7 528 reserelaterade denguefall, varav 3 135 krävde sjukhusvistelse och 19 resulterade i dödlighet.
(4) Expansion av vektorspridning: Globalt fortsätter det geografiska utbredningsområdet för Aedes aegypti och Aedes albopictus att expandera, och Aedes-myggor etablerar sig alltmer i delar av Europa. Följaktligen har dengue utvecklats från en traditionellt regional epidemi till ett globalt hot mot folkhälsan.
2.3 Mekanismer för samcirkulation av flera serotyper och reinfektion
Denguevirus består av fyra antigeniskt distinkta serotyper (DENV-1 till DENV-4). Infektion med en serotyp ger långvarig skyddande immunitet mot den specifika serotypen men endast tillfälligt och partiellt korsskydd mot de andra tre serotyperna. Den allmänna befolkningen är universellt mottaglig för DENV, där endast en delmängd av infekterade individer utvecklar klinisk sjukdom [2].
I endemiska regioner cirkulerar ofta flera DENV-serotyper samtidigt, vilket resulterar i att individer riskerar att drabbas av flera dengueinfektioner under sin livstid. WHO:s epidemiologiska studier har identifierat samcirkulation av flera serotyper som en viktig drivkraft för periodiska dengueutbrott [1].
2.4 Sekundärinfektion och antikroppsberoende förstärkning
Ett kritiskt och unikt fenomen inom dengueepidemiologi ärantikroppsberoende förstärkning (ADE)Vid sekundär infektion med en heterolog DENV-serotyp underlättar icke-neutraliserande antikroppar som produceras under den primära infektionen virusets inträde i monocyter och makrofager, vilket ökar virusreplikation. Denna mekanism är allmänt erkänd av WHO som en viktig patogen faktor vid svår denguefeber, inklusive hemorragisk denguefeber och denguechocksyndrom [1].
WHO:s epidemiologiska data visar konsekvent att individer med sekundär dengueinfektion har en signifikant högre risk att utveckla allvarlig sjukdom jämfört med de med primärinfektion – en egenskap som är av stor betydelse för sjukdomsövervakning och klinisk behandling. Det är viktigt att notera att även om risken för allvarlig sjukdom är förhöjd under sekundär infektion, kan infektion med vilken DENV-serotyp som helst potentiellt utvecklas till allvarlig dengue [1].
2.5 Icke-specifika kliniska manifestationer och risk för feldiagnos
De kliniska manifestationerna av dengue är anmärkningsvärt ospecifika, särskilt i tidiga stadier av sjukdomen, och överlappar ofta med de vid andra myggburna virusinfektioner (t.ex. chikungunya- och Zika-virus) samt vissa luftvägsinfektioner. WHO:s uppskattningar visar att 40–80 % av DENV-infektioner är asymptomatiska [3].
Typiska kliniska manifestationer inkluderar:
-Akut feber (som kvarstår i 2–7 dagar, kan vara bifasisk)
-Svår huvudvärk och retroorbital smärta (smärta bakom ögonen)
-Muskel- och ledvärk (vanligtvis kallad "benbrottsfeber")
-Makulata eller makulopapulära utslag
-Milda hemorragiska manifestationer (t.ex. ekkymos, epistaxis, tandköttsblödning)
Symtomatisk denguefeber delas vanligtvis in i tre distinkta faser: feberfasen, den kritiska fasen och återhämtningsfasen. Ungefär färre än 5 % av symtomatiska patienter utvecklar svår denguefeber. På grund av avsaknaden av specifika kliniska symtom är diagnos baserad enbart på kliniska symtom utmanande, vilket ökar risken för feldiagnos och underdiagnos. WHO betonar uttryckligen att klinisk diagnos ensam är otillräcklig för att säkerställa noggrannhet, vilket gör laboratoriebekräftelse oumbärlig [1].
3 viktiga punkter från WHO:s "Laboratorietester för denguevirus: Interimsriktlinjer, april 2025"
I april 2025 släppte Världshälsoorganisationen uppdaterade interimistiska riktlinjer för laboratorietester för DENV, som ger auktoritativ teknisk vägledning för global denguediagnos. Denna vägledning sammanfattar de senaste bevisen för laboratorietester av denguefeber i samband med den pågående globala denguekrisen och erbjuder praktiska rekommendationer anpassade till miljöer med varierande resursnivåer.

3.1 Grundläggande principer för teststrategi
Riktlinjerna betonar att denguediagnos måste tillämpa en kombinerad teststrategi med flera markörer baserad på sjukdomsstadiet [1]. Med tanke på avsaknaden av en universell diagnostisk algoritm bör teststrategierna anpassas till lokala epidemiologiska sammanhang, med hänsyn till följande nyckelfaktorer [1]:
-Infektionsstadium: Antalet dagar efter symtomdebut avgör den lämpligaste testmetoden.
-Provtyp: Lämpligheten av helblod, plasma eller serum för DENV-detektion
-Regional epidemiologi: De lokalt cirkulerande DENV-serotyperna och samcirkulation av andra arbovirus
-Risk för saminfektion: I regioner med överlappande arboviruscirkulation bör multiplextestning övervägas för att skilja mellan olika patogener.
3.2 Stegbaserad teststrategi
Enligt WHO:s riktlinjer bör laboratorietester för denguefeber följa tydliga tidsfönster baserade på sjukdomsstadiet [1,2]:
(1) Akutfastestning (≤7 dagar efter debut)
-Nukleinsyratestning (molekylär testning): Omvänd transkription-polymeraskedjereaktion (RT-PCR) och andra molekylära metoder detekterar DENV-RNA med hög känslighet.
-Antigentestning: NS1-antigendetektion, som blir detekterbar inom 1–3 dagar efter debut.
Under den akuta fasen är vireminivåerna relativt höga, och testning av nukleinsyra och antigen uppnår optimal känslighet.
(2) Testning i konvalescentfasen (≥4 dagar efter debut)
-Serologisk testning: IgM-antikroppar blir vanligtvis detekterbara runt dag 4 efter debut.
-I de flesta fall kvarstår IgM-antikroppar i 14–20 dagar, och i vissa fall kan kvarståndet vara upp till 90 dagar.
-IgG-testning har begränsat värde för diagnos av akut denguefeber på grund av potentiella korsreaktiva antikroppar från tidigare flavivirusinfektion eller vaccination.
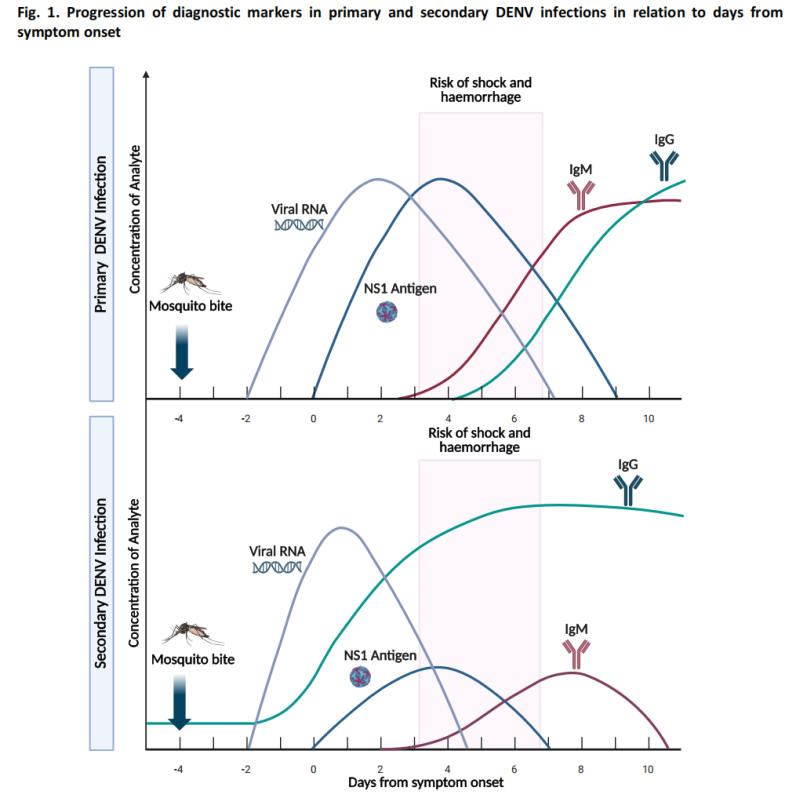
(3) Diagnostisk algoritm för misstänkta fall
Vägledningen innehåller en diagnostisk algoritm för misstänkta denguefall och rekommenderar lämpliga testmetoder baserat på dagar efter symtomdebut: NS1-antigentestning och nukleinsyratestning är de primära metoderna i den tidiga fasen, medan serologisk testning är den primära metoden i den senare fasen.
3.3 Utvärdering och val av testmetodens prestanda
Enligt WHO är en systematisk utvärdering av prestandan och tillämpliga scenarier för olika denguetestningar följande:
| Testmetod | Mål | Tidsfönster | Primärt applikationsscenario | Överväganden |
| Nukleinsyratestning | Viralt RNA | 1–7 dagar efter debut | Tidig bekräftelse, serotypidentifiering | Guldstandardmetoden; kräver specialiserad laboratorieutrustning och teknisk expertis |
| NS1-antigentestning | Icke-strukturellt protein | 1–3 dagar efter debut | Tidig snabbscreening | Tillgänglig i snabbdiagnostiskt testformat (RDT), lämplig för resursbegränsade miljöer |
| IgM-antikroppstestning | Specifika IgM-antikroppar | ≥4 dagar efter debut | Diagnos av nyligen infektion | Ett enda serumprov tyder endast på en möjlig nyligen genomförd infektion; serokonversion krävs för bekräftelse |
| IgG-antikroppstestning | Specifika IgG-antikroppar | Konvalescent/tidigare infektion | Epidemiologisk undersökning, bedömning av immunitetsstatus | Ett enda serumprov är inte lämpligt för diagnos av akut denguefeber |
| Kombinerad testning (NS1+IgM/IgG) | Antigen + Antikroppar | Fullständigt sjukdomsförlopp | Omfattande diagnos av dengueinfektion | För närvarande det bäst presterande RDT-formatet för denguediagnos |
| NGS | Viralt RNA | 1–7 dagar efter debut | Viral genomisk övervakning | Kräver specialiserad sekvenseringsutrustning och bioinformatisk analyskapacitet |
4 rekommendationer för makro- och mikrotest av denguedetekteringsprodukter per scenario
För att stödja förebyggande och kontroll av denguefeber tillhandahåller Macro & Micro-Test en integrerad diagnostisk portfölj som omfattar snabb screening, molekylär bekräftelse och genomisk övervakning, och möter behov i olika faser av utbrottshantering.
4.1 Scenario 1: Snabb screening och riktad övervakning
Gäller febermottagningar, primärvårdsinrättningar, screening för utbrott i samhället och karantän i hamnar/gränser.
-Snabbtest för denguevirus NS1-antigen: Upptäcker tidig infektion (1–3 dagar efter sjukdomsdebut) med resultat inom 15 minuter för snabb triage.
-Denguevirus IgM/IgG-antikroppstest: Skiljer mellan primära/sekundära infektioner för att utvärdera risken för allvarlig sjukdom.
-Denguevirus NS1-antigen + IgM/IgG kombinerat snabbtest: Detekterar antigen och antikroppar samtidigt för fullständig diagnos.
-Chikungunyavirus IgM/IgG-antikroppstest: Möjliggör differentialdiagnos med denguefeber för att identifiera patogener korrekt.
4.2 Scenario 2: Precisionsdiagnos och akutinsatser
-Denguevirus I/II/III/IV Nukleinsyradetekteringskit: Detekterar och differentierar 4 serotyper (detektionsgräns 500 kopior/ml) för spårning av utbrott.
-Frystorkat denguevirus PCR-kit: Kan transporteras i rumstemperatur, lämplig för resursbegränsade områden och plötsliga utbrott.
-Dengue/Zika/Chikungunya Multiplex Real-Time PCR Kit: Detekterar samtidigt 3 arbovirus för effektiv differentialdiagnos vid komplexa utbrott.

Alla ovanstående reagenser är kompatibla med AIO 800 helautomatiska prov-till-svar-system, vilket minskar manuell drift och korskontaminering, samt förbättrar effektivitet och biosäkerhet.
4.3 Scenario 3: Genomövervakning och analys av viral härstamning
Tillämplig på nationella referenslaboratorier och forskningsinstitutioner för folkhälsa, i linje med WHO:s ståndpunkt för NGS.
Macro & Micro-Tests lösningar för genomövervakning stöder helgenomsekvensering för virusspårning, klargörande av överföringskedjor, variantövervakning och justering av vaccinstrategier. De stöder manuella/automatiserade arbetsflöden, vilket förbättrar genomströmning och reproducerbarhet, vilket gör det möjligt för laboratorier att uppgradera från rutintestning till avancerad övervakning, i linje med WHO:s betoning på att stärka övervakningen av virusutveckling.

4.4 Värdet av integrerade lösningar
Macro & Micro-Test erbjuder kompletta diagnostiska lösningar för detektion av arbovirus, som stöder varje steg i utbrottshanteringen: snabba screeningsverktyg för primärvård, molekylär bekräftelse för precisionsdiagnos och helgenomanalys för epidemiologisk övervakning. Med högpresterande analyser, flexibla arbetsflöden och automatiseringsklara plattformar ger dessa lösningar laboratorier och folkhälsosystem möjlighet att stärka beredskapen och responsen på nya arbovirushot över hela världen.
Referenser
[1] Världshälsoorganisationen. Laboratorietester för denguevirus: Interimsriktlinjer, april 2025. Genève: Världshälsoorganisationen; 2025.
[2] WHO:s tekniska rådgivande grupp för globalt arbovirusinitiativ. Stärka den globala beredskapen och insatserna mot hot från arbovirussjukdomar: En uppmaning till handling. Lancet Infect Dis. 2026;26(1):15-17.
[3] Lancetmikroben. Att övervinna dilemmat med denguediagnostik. Lancetmikroben. 2025;6(7):101190.
Publiceringstid: 20 mars 2026
